KİMYA VE E 5. Aşağıda bir elektrokimyasal pil düzeneği verilmiş- tir. 000 moon Tuz köprüsü -Cu(k) Na(K) 20 25 °C 1M Na+ (suda) 25 °C 1M Fe2+ (suda) 25 °C 1M Fe3+. (

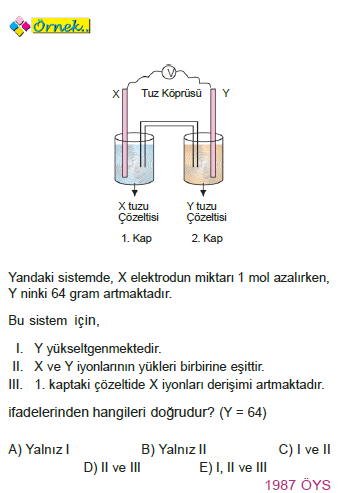
ADASI Örnek: Anot kotor. Zn Tuz köprüsü Cu 1M ZnSO4 1M CuSO4 I. kap II. kap Zn → Zn+2 + 2e- E = +0,76 V Cu Cu+2 + 2e £° = -0,34

Silimleri 12. 104 Elektrokimyasal piller ile ilgili, I. Anotta yükseltgenme olur. II. Anot elektrodun kütlesi azalır.
ELEKTROKİMYASAL PİLLER KONUSUNUN ÖĞRETİMİNDE KAVRAM KARİKATÜRLERİNİN KULLANIMI USING CONCEPT CARTOONS IN THE TEACHING
![10. Bir elektrokimyasal pil sistemine ait Nernst denklemi aşağıda verilmiştir. Epii = Epil 0,06 [Mg2+] log 2 [Cu+12 Buna göre; 1. Pil şeması Mg(k) / Mg2+(suda) // 2Cu+(suda) / 2Cu(k) şeklindedir. II._Mo 10. Bir elektrokimyasal pil sistemine ait Nernst denklemi aşağıda verilmiştir. Epii = Epil 0,06 [Mg2+] log 2 [Cu+12 Buna göre; 1. Pil şeması Mg(k) / Mg2+(suda) // 2Cu+(suda) / 2Cu(k) şeklindedir. II._Mo](https://media.kunduz.com/media/question/seo/raw/20220221144742773394-1842388_qBSX7Wi3N.jpeg)
10. Bir elektrokimyasal pil sistemine ait Nernst denklemi aşağıda verilmiştir. Epii = Epil 0,06 [Mg2+] log 2 [Cu+12 Buna göre; 1. Pil şeması Mg(k) / Mg2+(suda) // 2Cu+(suda) / 2Cu(k) şeklindedir. II._Mo
ELEKTROKİMYASAL PİLLER KONUSUNUN ÖĞRETİMİNDE KAVRAM KARİKATÜRLERİNİN KULLANIMI USING CONCEPT CARTOONS IN THE TEACHING
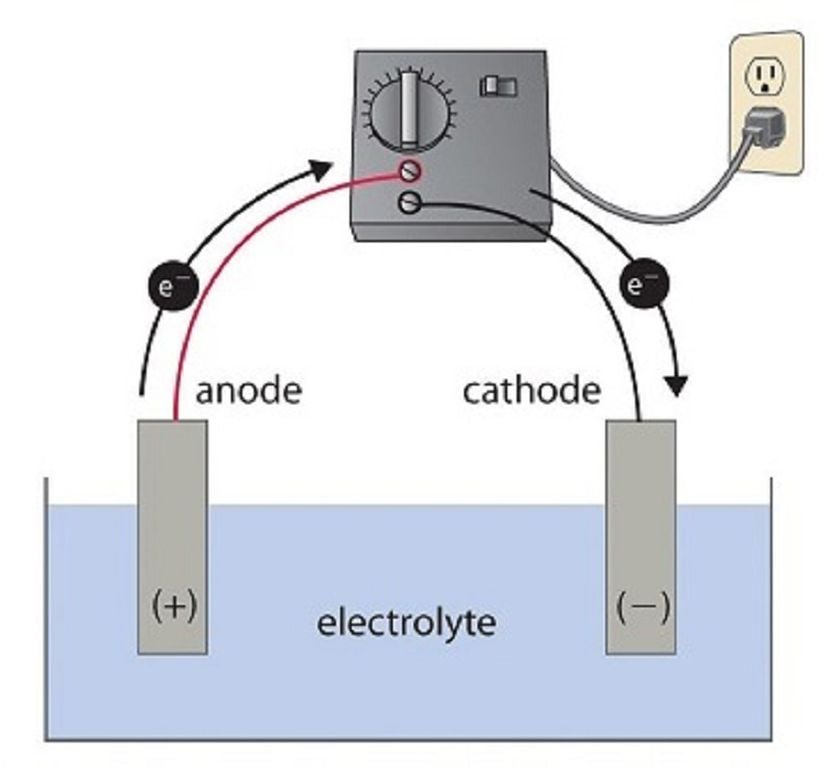
Elektrokimyasal Piller Nasıl Çalışır? Galvanik (Voltaik) Hücrelerin Çalışma Prensipleri Nelerdir? - Evrim Ağacı